上篇

1.FDA对电子烟出口监管的背景与目的
电子烟市场的迅速发展在全球范围内引起了广泛关注。根据美国疾病控制与预防中心(CDC)的数据,电子烟使用率在美国中学生中增长了近80%。这种激增引发了对电子烟的安全性和监管的担忧。
作为美国主要的食品和药品监管机构,FDA(Food and Drug Administration 食品与药品监督管理局)负责确保美国市场上的产品安全、有效和合规。在电子烟出口市场中,FDA的监管角色变得至关重要;而FDA对于电子烟的管理,是为了更好的干预乃至控制以下几个重大风险:
1)健康风险:电子烟的健康风险仍然存在争议。尽管电子烟相对于传统香烟可能含有较少的有害物质,但仍然存在与电子烟使用相关的健康问题,例如呼吸道疾病和肺损伤。这些健康风险引发了对电子烟产品质量和安全性的关注,需要监管机构对其进行严格监管。
2)青少年使用率增加:电子烟的广泛推广和市场营销活动导致了青少年使用率的增加。根据CDC(美国疾病控制与预防中心)数据,2019年,约5,400,000名中学生和2,300,000名高中生在过去30天内使用了电子烟。在FDA严格执法管理下,这一数字获得明显向好转化,据公开调研数字显示,2023年美国高中生吸烟同比下降10%左右。
3)电子烟产品缺乏标准化和一致性:由于电子烟市场的相对年轻和快速发展,产品标准和规定的缺乏导致了产品质量和安全性的不确定性。不同国家和地区对电子烟的监管政策存在差异,缺乏一致的标准和规定。这使得监管机构面临挑战,需要制定更加全面和严格的监管政策来确保产品质量和安全。
4)市场透明度和消费者保护:FDA的监管作用不仅仅关注产品质量和安全性,还涉及市场透明度和消费者保护。监管机构需要确保电子烟产品的标签和包装信息准确、清晰,并限制对产品的误导性广告和宣传。这将有助于消费者做出明智的购买决策,保护其权益和健康。
2.FDA主要监管手段与程序
FDA于2016年根据FDCA以及《美国联邦法规》(Code of Federal Regulations, CFR)第21章的规定设立的一套关于新烟草产品上市前的审核程序PMTA(Pre-Market Tobacco Application),电子烟产品需通过提交PMTA程序文件并通过审批以获得FDA发布的营销许可。
PMTA要求烟草企业向FDA提交详细的科学数据和信息,以证明其产品对公众健康的潜在风险极低,并且产品的益处超过了潜在的风险。这个审核程序旨在确保新烟草产品的安全性和合规性。另外,烟草制造商或供应商在申请过程中可以向FDA提交TPMP(Tobacco Products Master File)作为PMTA的辅助说明文件,以系统性提供关于产品成分、制造过程、质量控制等方面的信息,支持产品的安全性和合规性的评估,从而帮助FDA更好地了解和评估烟草产品的性质和特征。

3.PMTA的主要内容
PMTA政策旨在保护公众的健康和安全,并确保电子烟产品在市场上的合规性。对于违反FDA规定的电子烟制造商和出口商,FDA有权采取一系列的制裁措施,包括发出警告信、罚款、产品召回或禁止销售等。这些措施旨在维护市场的合规性和公众的健康安全。根据FDA的数据,已经对数十家电子烟制造商和出口商采取了制裁措施,这显示了FDA对于电子烟监管的严格和有效。
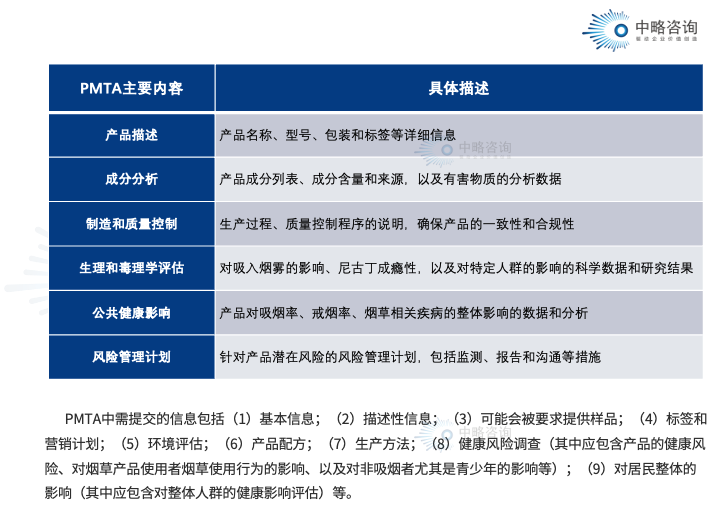
制造商和出口商需要提交详细的申请,进行必要的测试和验证,并遵守FDA对质量、安全性、标签和包装、广告宣传等方面的要求和限制;FDA对违规行为采取制裁措施,以维护市场的合规性和公众的健康安全。
作为该审批的主管部门,FDA有权对不符合要求的申请做出拒绝,拒绝的PMTA的理由包括:(1)申请人无法证明允许该烟草产品投入市场有利于公共健康的保护;(2)在生产、加工、包装该烟草产品的过程中不符合FDCA对生产规范的规定;(3)标签错误或有误导性;(4)该烟草产品不符合FDCA对产品标准的规定,且没有偏离该标准的恰当理由。
除被拒绝受理、拒绝提交或发布营销拒绝令的PMTA外,实务中若PMTA还在审查中,且企业提交的PMTA向FDA表明产品不会吸引青少年,则一般会被默许销售。
本报告旨在系统地探究FDA对电子烟出口监管的政策趋势,并为相关企业提供指导和建议。为达到这一目标,中略咨询采用了以下方法:
1) 文献研究和分析:对FDA关于电子烟出口监管的相关政策文件进行全面研究和分析,包括指导文件、规定和公告,以及与电子烟出口相关的法律法规。
2) 市场调研:收集电子烟行业的最新数据和趋势,分析市场规模、增长率、消费者使用行为等关键指标,以了解市场现状和未来发展趋势。
3) 政策比较研究:对国内外相关监管机构对电子烟出口的政策进行比较研究,了解FDA在全球范围内的监管地位和趋势。
随着对FDA电子烟出口监管政策的深入分析,我们已经为理解这一复杂领域打下了坚实的基础。在接下来中篇的内容中,我们将探讨这些政策的监管成效以及它们对未来市场趋势的影响。敬请期待,我们将一一剖析中国企业如何在这个不断变化的监管环境中找到立足点!

注释:
电子烟作为一种替代传统烟草产品的新型产品,近年来在全球市场呈现出快速增长的趋势。根据权威机构Euromonitor International的报告,截止2023年一次性电子烟占全球电子烟市场的近40%,2023年电子烟市场规模预计为267.6亿美元,预计到2028年将达到501.6亿美元,在预测期内(2023-2028年)复合年增长率为13.39%,这一数据清晰地揭示了电子烟市场的巨大潜力和吸引力。
近年来我国开始重视对电子烟企业的监管,且已经开始对中国企业向境外出口电子烟的行为实施监管。烟草专卖局2023年7月20日发布的《关于推动出口电子烟产品质量保证体系建设的指引》(以下简称“《出口指引》”)第十四条规定,出口电子烟产品因质量安全问题被国际组织、境外政府机构通报的,企业应当立即向所在地烟草专卖局报告,相关企业应当接受烟草专卖局依法组织开展的核查处理。
美国作为全球电子烟第一大消费市场,同时也是全球电子烟市场的风向标。美国疾病控制与预防中心的数据显示,一次性电子烟约占美国电子烟市场的53%,自2020年以来规模增长了一倍多。因此,美国FDA对于电子烟的监管早在2016年开始进行,当时FDA宣布将对电子烟产品进行类似于传统烟草产品的监管。为了加强对电子烟出口的监管,FDA于2019年发布了《电子烟产品出口监管规定》。该规定要求电子烟生产商和出口商在出口前必须获得FDA的许可,并要求产品标签和包装上必须包含警示语句和成分清单,以及禁止向18岁以下的未成年人销售电子烟产品,并要求零售商采取措施确保购买者的年龄符合法定要求。随着对电子烟出口监管的进一步加强,FDA还在不断研究和评估电子烟的健康风险,并积极寻求公众和专家的意见和建议。